Reacciones Químicas
Espuma que arde:
Cubrir un clavo de hierro de cobre:
Neutralización ácido-base:
Cómo hacer queso casero:
| Enlaces entre átomos |
Prácticamente todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las intensas fuerzas que mantienen unidos los átomos en las distintas sustancias se denominan enlaces químicos. ¿Por qué se unen los átomos? Los átomos se unen porque, al estar unidos, adquieren una situación más estable que cuando estaban separados. Esta situación de mayor estabilidad suele darse cuando el número de electrones que poseen los átomos en su último nivel es igual a ocho, estructura que coincide con la de los gases nobles.Podemos explicar la unión de los átomos para formar enlaces porque con ella consiguen que su último nivel tenga 8 electrones, la misma configuración electrónica que los átomos de los gases nobles. Este principio recibe el nombre de regla del octeto y aunque no es general para todos los átomos, es útil en muchos casos. Distintos tipos de enlaces 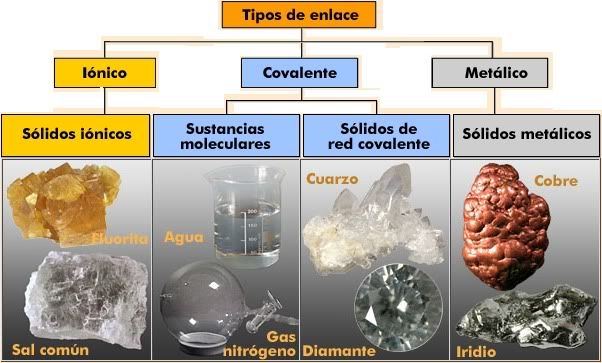 Enlace iónico |
| Los enlaces covalentes son las fuerzas que mantienen unidos entre sí los átomos no metálicos. Estos átomos tienen muchos electrones en su nivel más externo (electrones de valencia) y tienden a ganar electrones para adquirir la estabilidad de la estructura electrónica de gas noble. Los átomos no metálicos no pueden cederse electrones entre sí para formar iones de signo opuesto. El enlace se forma al compartir un par de electrones entre los dos átomos, uno procedente de cada átomo. El par de electrones compartido es común a los dos átomos y los mantiene unidos, adquiriendo la estructura electrónica de gas noble. Así se forman normalmente las moléculas.
|